- Labor
- Labormedizin
- Reagenz / als Lösung
- Charles River Laboratories
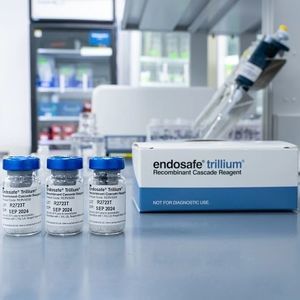
Reagenz für Endotoxine Endosafe® LALals Lösungfür MikrobiologieBakterien
Zu meinen Favoriten hinzufügen
Zum Produktvergleich hinzufügen
Eigenschaften
- Typ
- als Lösung
- Anwendung
- für Mikrobiologie
- Getesteter Marker
- für Endotoxine
- Getesteter Mikroorganismus
- Bakterien
- Methode
- chromogen
- Weitere Eigenschaften
- analysiert
Beschreibung
Herkömmliche Endotoxin-Tests waren in der Vergangenheit mit vielen Problemen verbunden, darunter lange Durchlaufzeiten, umfangreiche Schulungen und mehrere Schritte zur Testvorbereitung. Erschwerend kommt hinzu, dass ein ungültiges LAL-Testergebnis den Zeitplan für Ihre Produktion gefährden kann.
Die Endosafe LAL-Kartuschentechnologie ist die innovative Antwort auf den Bedarf an präziseren, objektiveren und schnelleren quantitativen Ergebnissen bei der kinetisch-chromogenen Methode. Unsere Endosafe LAL-Kartuschen sind eine neuartige Technologie zur Optimierung und Verfeinerung der LAL-Nutzung. Sie verbrauchen 95 % weniger Hufeisenkrebs-Rohmaterial und Zubehör als die Gel-Klotz- und KTA-Methoden. Die Einwegkartuschen enthalten präzise Mengen unseres von der FDA lizenzierten chromogenen LAL-Reagenz, chromogenen Substrats und Kontrollen, die zur Messung der Farbintensität in direktem Zusammenhang mit der Endotoxinkonzentration in einer Probe benötigt werden, um schnelle und genaue Ergebnisse zu erhalten.
Endosafe LAL-Kartuschen sind eine kompromisslose BET-Methode
Bei den von der FDA zugelassenen Endosafe LAL-Kartuschen handelt es sich um eine kinetische chromogene LAL-Methode, die in der EP/USP spezifiziert ist.
Sie führen automatisch eine Doppelprobe und eine positive Produktkontrolle durch und erfüllen die harmonisierten BET-Kapitel der USP oder Ph.Eur. für LAL-Tests.jede Kartusche wird nach strengen Qualitätskontrollverfahren hergestellt, um die Testgenauigkeit und Produktstabilität zu gewährleisten, und entspricht den bestehenden weltweit harmonisierten regulatorischen Richtlinien
Da die Kartuschen vorgefüllt sind, entfällt die tägliche manuelle Vorbereitung von Standards und Reagenzien. Die Konsolidierung aller wesentlichen Komponenten in einer eigenständigen Kartusche reduziert die Pipettierschritte, verringert die Testvariabilität, die Kreuzkontamination, das Risiko falsch positiver Ergebnisse und die Anzahl der Wiederholungstests.
---
Kataloge
Für dieses Produkt ist kein Katalog verfügbar.
Alle Kataloge von Charles River Laboratories anzeigenWeitere Produkte von Charles River Laboratories
Bacterial Endotoxin Testing
Verwandte Suchbegriffe
- Reagenzkit
- Testkit
- Reagenzkit / als Lösung
- Flüssiges Reagenzkit
- Immunologischer Testkit
- Labor-Reagenzkit
- Testkit für Infektionskrankheiten
- Analysesoftware
- Enzyme-Reagenzkit
- Pufferlösungs-Reagenzkit
- Steuerungssoftware
- ELISA-Kit
- Laborsoftware
- Reporting-Software
- Bakterien-Reagenzkit
- IgG-Testkit
- Testkit für Zellen
- Monitoring-Software
- Automatisierte Software
- Software für Krankenhaus
* Die Preise verstehen sich ohne MwSt., Versandkosten und Zollgebühren. Eventuelle Zusatzkosten für Installation oder Inbetriebnahme sind nicht enthalten. Es handelt sich um unverbindliche Preisangaben, die je nach Land, Kurs der Rohstoffe und Wechselkurs schwanken können.